
Ирина Якутенко
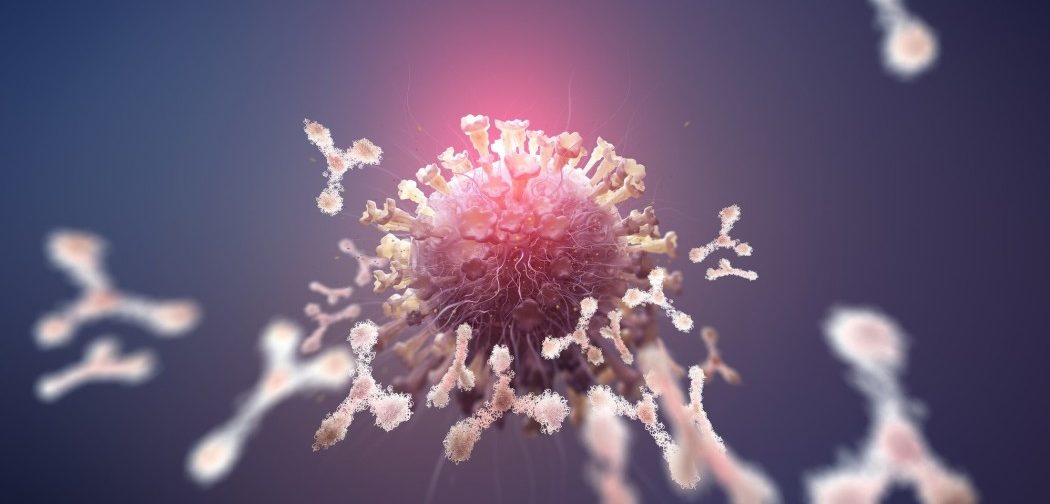
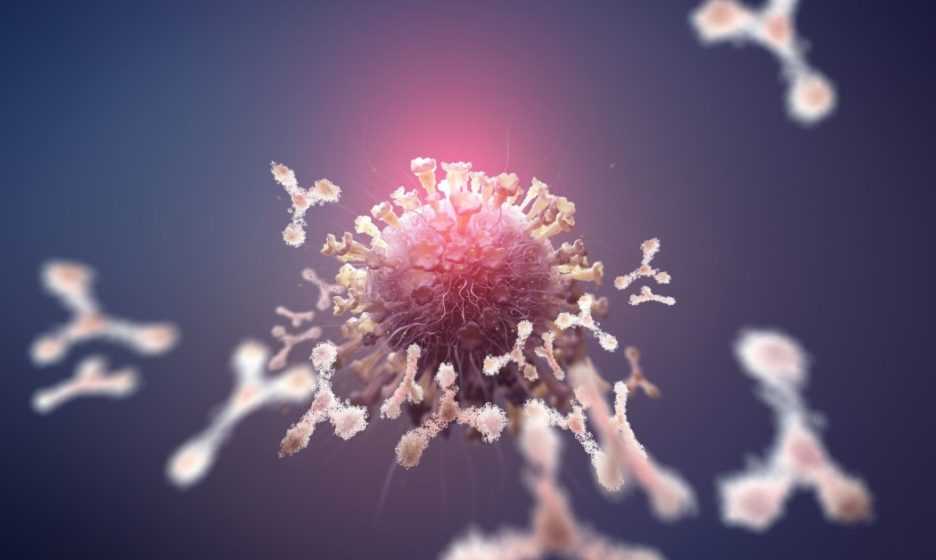
Антитела — это белки, составленные из нескольких полипептидных цепей. Отдельное антитело по форме напоминает букву Y. Рожки игрека предназначены для того, чтобы узнавать и крепко приклеиваться к чужеродным молекулам или их фрагментам, а ножку распознают различные иммунные клетки.
Задача антител — находить в организме чужеродные элементы и прицепляться к ним. В некоторых случаях такое связывание само по себе обезвреживает врага — если, например, прикрепившиеся к вирусным частицам антитела физически блокируют белок, при помощи которого патоген соединяется с клеточными структурами (антитела, способные на такое, называют нейтрализующими).
Но гораздо чаще антительные метки служат сигналом для других компонентов иммунной системы, в первую очередь макрофагов: они видят торчащую ножку Y, а точнее — множество торчащих ножек, и немедленно уничтожают подозрительный объект, к которому она прикреплена. Без таких меток найти врага клеткам-убийцам гораздо сложнее.
Антитела синтезируются особой разновидностью лимфоцитов — B-клетками. Благодаря хитрым мутационным процессам, изменяющим только строго выделенные части генома предшественников B-клеток, в нашем организме исходно, еще до встреч с любыми патогенами, присутствуют миллиарды типов B-лимфоцитов, которые готовы производить антитела, узнающие миллиарды же типов чужеродных (то есть тех, которых нет в наших клетках) молекулярных мотивов.
Как антитела нас защищают
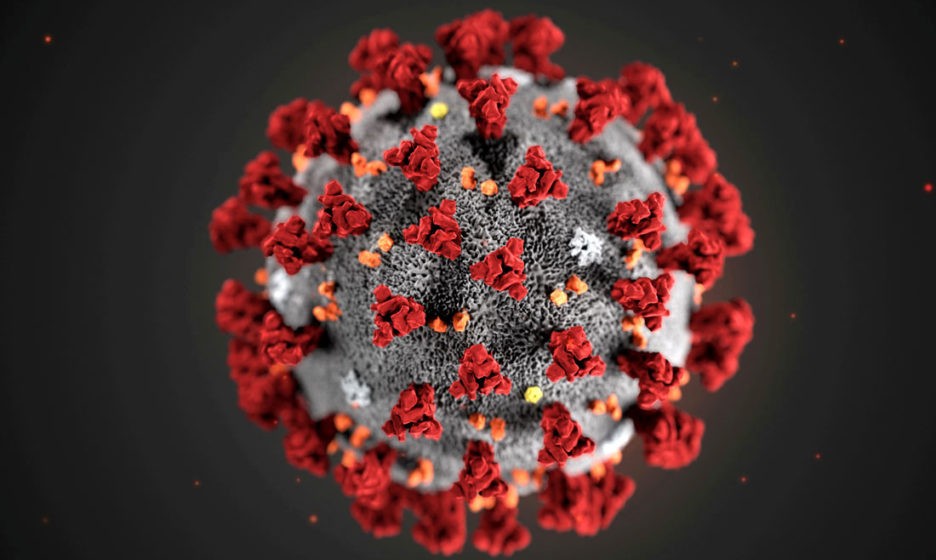
Когда в организм попадает вирус, бактерия, простейшее или другой потенциальный враг, какое-нибудь из антител обязательно узнает тот или иной вражеский фрагмент — его называют антиген — и прилепится к нему. Такие исходные антитела не плавают в крови, а встроены в мембрану B-клеток, и, после того как рожки свяжут антиген, B-клетка активируется и начинает бешено делиться . Ее потомки производят и выделяют только правильные антитела, узнающие именно этот антиген, более того, в них запускается тот самый хитрый мутагенез, благодаря которому каждый раз синтезируются игреки с немного видоизмененными рожками. По теории вероятностей какие-то из них будут связывать антиген лучше изначальных — и дальше делиться и производить новые антитела будут уже потомки этой клетки.
Благодаря такой селекции к концу болезни в организме начинают синтезироваться сверхточные антитела, идеально узнающие конкретного врага. После победы в организме остаются так называемые B-клетки памяти, которые хранят инструкции по производству именно этих антител. Если через какое-то время тот же патоген вновь попытается проникнуть внутрь, синтез специфичных, максимально липучих антител будет запущен сразу, а не через пару недель, как при первой встрече.
Антитела делятся на пять типов, каждый из которых заточен на выполнение своих задач.
«Классические» антитела в форме Y — это IgG. Они путешествуют по организму в плазме крови, очень точно узнают свой антиген (то есть реагируют на один, и только один конкретный фрагмент) и намертво прилипают к нему. IgG начинают синтезироваться в больших количествах в среднем на 10–14 день от начала болезни — это продукт той самой мутационной «подстройки» и отбора B-клеток.
Первыми на незнакомый патоген реагируют IgM. Это неспецифические антитела, они узнают множество теоретически возможных антигенов, но не настроены на какой-то конкретный. В отличие от одиночек IgG, молекулы этого типа антител плавают впятером: они сцеплены за «ножки» и образуют красивую звезду. Благодаря такой форме узнающие антиген рожки торчат в разные стороны — это позволяет IgM «склеивать» чужеродные объекты даже несмотря на то, что связывание с ними может быть не очень прочным. Также IgM могут выполнять роль рецепторов на поверхности B-клеток: с их помощью эти лимфоциты узнают «свои» антигены.
Антитела, работающие преимущественно не в крови, а на слизистых и в секретируемых жидкостях, — IgA. Это специфические антитела, то есть они образуются к конкретному антигену после того, как организм познакомится с ним. По этой причине у новорожденных нет своих иммуноглобулинов типа A, но они в большом количестве получают их из материнского молока. Постепенно у младенцев вырабатываются собственные IgA: уже к году их количество составляет примерно 20% от взрослой нормы и полностью достигает ее к 4–6 годам [27].
Большая часть IgA синтезируется в виде скрепленных «ножками» димеров, реже они встречаются в полимерной или одиночной форме. Роль иммуноглобулинов типа А в плазме крови ясна не до конца, но в последние годы ученые находят все больше доказательств, что они принимают важное участие в регуляции иммунного ответа, в том числе модулируя как воспалительные, так и противовоспалительные процессы [28].
Иммуноглобулины типа E были предназначены для борьбы с крупными паразитами вроде червей, причем не с привычными и относительно безобидными острицами или аскаридами, а с теми, что живут в тканях и могут легко убить хозяина. В современном западном обществе такая напасть встречается редко, IgE простаивают и от безделья занимаются нападением на безвредные антигены типа пыльцы или кошачьей шерсти, стимулируя процессы, приводящие к аллергиям.
Функции IgD известны слабо: они могут выполнять функции рецепторов на незрелых B-клетках и секретироваться в плазму вместе с IgM. Предполагается, что этот тип антителможет участвовать в борьбе как раз с респираторными инфекционными агентами [29].
Что такое клеточная ветвь иммунитета
Хотя основное внимание в медийном поле, да и в научных публикациях, уделяется антителам против коронавируса, это не единственная линия защиты. Помимо антительного иммунного ответа (ученые говорят «гуморального»), при встрече с патогеном у нас активируется так называемая клеточная ветвь иммунитета.
Более того, именно она включается первой: организм по умолчанию старается справиться с патогеном малыми силами, не беспокоя В-клетки и всю громоздкую махину выработки антител.
По этому сначала активируется система врожденного иммунитета, потом Т-клеточная ветвь, и, только если все это не помогло, начинается синтез антител. Компоненты клеточной составляющей иммунитета тоже умеют узнавать вирусные фрагменты и запускать цепочку реакций, приводящей к тому, что клетки-убийцы уничтожат клетки-жертвы, в которых завелся вирус.
Аналогично с активацией антительного иммунного ответа, после того как Т-клетки и компания выиграют битву с вирусом, в организме сохранятся клетки памяти (Т-клетки памяти, в противовес В-клеткам памяти, остающимся после 9 На самое деле все еще сложнее: и гуморальная, и клеточная составляющие могут быть врожденными или приобретенными. В этих двух случаях участники цепочек защитных реакций будут совершенно разными (скажем, приобретенная гуморальная компонента — это антитела, а врожденная — всевозможные лизоцимы).
Но в данном случае нам нет смысла вдаваться в эти детали, тем более что при активации клеточной ветви иммунитета при вторжении SARS-CoV-2 активируются как врожденные, так и приобретенные механизмы выработки гуморального ответа). И при следующей встрече с тем же вирусом они немедленно активируются и очень быстро запустят защитный ответ.
Если совсем упрощать, то антитела не дают вирусу заражать новые клетки, а клеточная ветвь иммунитета отвечает за уничтожение тех клеток, которые уже инфицированы. Для полноценной защиты идеально, чтобы работали оба направления.
Проблема в том, что увидеть, запускалась ли у человека клеточная ветвь иммунитета, намного сложнее, чем определить, имел ли место гуморальный ответ. Последний проверяют довольно простым тестом на антитела. Чтобы выяснить, есть ли у пациента клеточная память, нужно проводить длительные и трудоемкие исследования. Они требуют специально обученных сотрудников, оборудования и так далее — всего этого в обычных диагностических медицинских лабораториях нет.
Тех, кто справился с вирусом, может быть больше
Не в последнюю очередь по этой причине в медучреждениях стандартно проводят проверку на антитела, а не на признаки активации клеточного иммунитета. Однако нельзя исключать, что у какой-то части людей организм справился с SARS-CoV-2 только силами клеточного иммунитета (или, по крайней мере, именно работа этой системы имела определя ющее значение) — и процент таких людей может быть существенным.
Первая более или менее серьезная работа на эту тему появилась только в конце июня 2020 года, через полгода после начала эпидемии. Шведские ученые из Каролинского университета в Стокгольме проверили, был ли Т-клеточный ответ у больных COVID-19 с выраженными симптомами, со слабыми симптомами и без симптомов, а также изучили донорскую кровь, собранную в мае 2020 года (сдававшие ее добровольцы были уверены, что ничем таким подозрительным не болели) [30], [31]. И оказалось, что Т-клеточный ответ имел место у всех переболевших и примерно у 30% доноров.
При этом антитела детектировались лишь у тех, кто болел явно выраженной коронавирусной инфекцией, причем чем сильнее проявлялись симптомы, тем более заметным был титр.
И это не первое подтверждение того, что у многих достоверно переболевших COVID-19 не наблюдается значимого титра антител [32]. Эти данные говорят нам сразу о нескольких вещах.
Во-первых, COVID-19 переболело существенно больше людей, чем мы выявляем ПЦР-тестом, КТ и даже тестом на антитела.
Это хорошо, так как приближает коллективный иммунитет и само по себе замедляет распространение инфекции: поборовшие вирус силами Т-клеточного иммунитета, вполне вероятно, смогут сделать это еще раз до того, как вирус как следует размножится, а носители начнут быть заразными.
Впрочем, конкретно с этим выводом стоит быть осторожнее, так как мы не знаем, с чем связано наличие только Т-клеточного ответа. Возможно, эти люди изначально получили малую дозу вируса и поэтому смогли справиться с ним без привлечения антител. Не исключено, что при большем забросе вируса они все же заболеют, но, вероятно, не очень тяжело, так как натренированная клеточная составляющая во второй раз активируется еще быстрее.
Кроме того, явное наличие Т-клеточного ответа требует более внимательного подхода к разработке вакцин. Главным критерием их эффективности часто — а особенно сейчас, в условиях чрезвычайной спешки, — является способность стимулировать выработку антител. На клеточную компоненту, конечно, смотрят, но по-прежнему ориентируются в основном на антитела.
Однако нельзя исключать, что вакцина, дающая хороший титр, но не подстегивающая клеточную компоненту, может обеспечивать не слишком надежную защиту. Вполне возможно, что вакцина, которая заставляет активироваться именно эту ветвь иммунитета, окажется куда более действенной.
Различные паттерны развития иммунного ответа при вторжении SARS-CoV-2 — высокий или низкий титр антител, отсутствие их у переболевших или наличие у тех, кто не чувствовал никаких симптомов, признаки активации клеточной компоненты, в том числе у вроде бы неболевших, — свидетельствуют о сложном взаимодействии вируса и различных составляющих иммунитета.
Нам только предстоит выяснить, в какой степени и когда в борьбу с патогеном вовлекается клеточный иммунитет, почему у одних людей он справляется с вирусом единолично, а другим — в том числе и бессимптомным — приходится подключать антитела и так далее. Строго говоря, мы не знаем ответов на эти вопросы и для остальных простудных вирусов, более того, для большинства из них мы в принципе плохо представляем, как выглядит динамика иммунного ответа.
Возможно, эпидемия COVID-19 подстегнет исследования в этом направлении, потому что, как выясняется, даже бесполезные знания о неопасных вирусах однажды могут очень пригодиться.